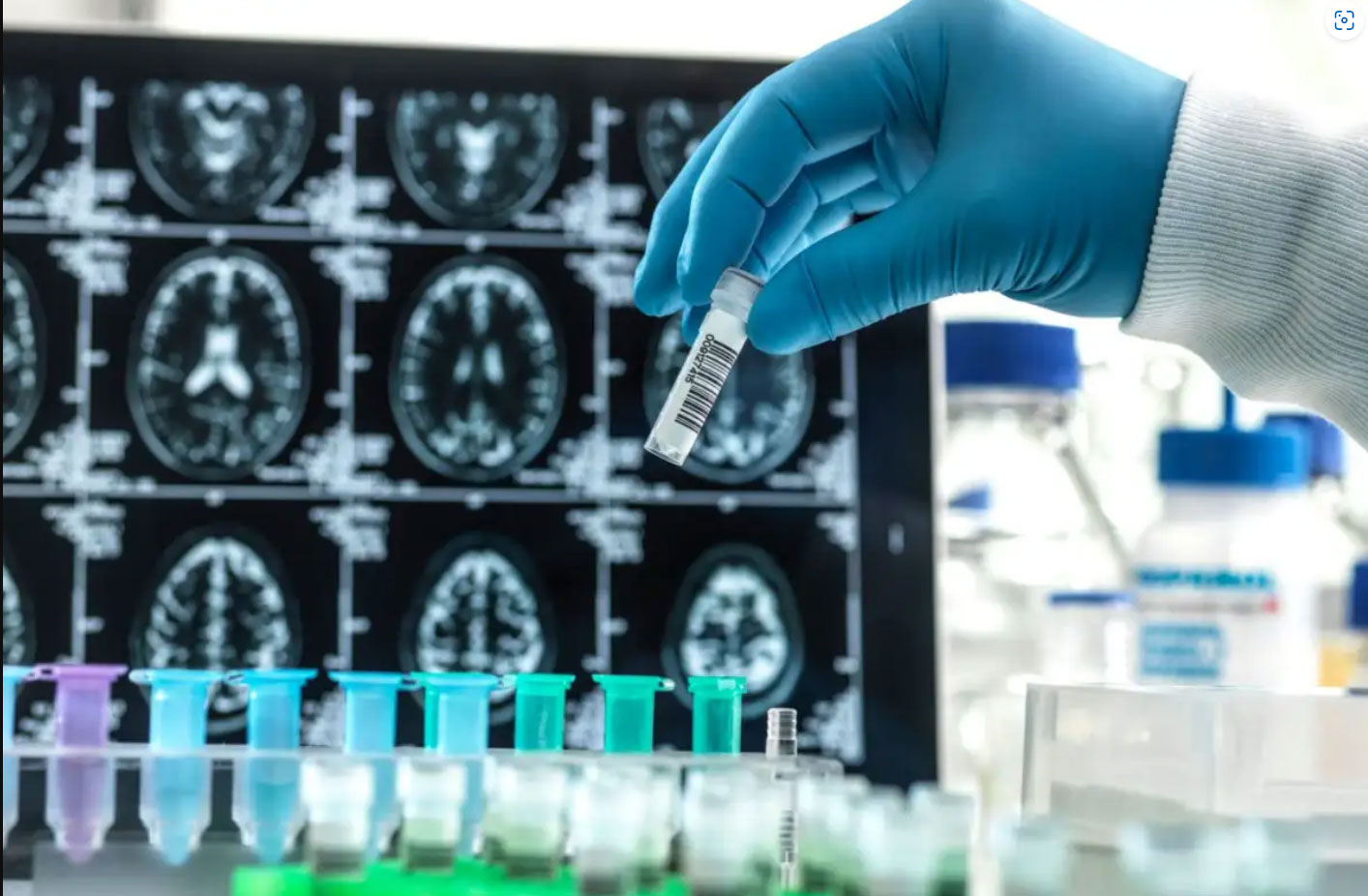
نتایج آزمایشی داروی Lecanemab روی 1795 نفر منتشر شد که نشان میدهد روند زوال ذهن در بیماران آلزایمر که در مراحل اولیه هستند، کند میشود.
نتایج امیدوارکننده به داروی جدید علیه آلزایمر
به گزارش آی زندگی و به نقل از دیلی میل، داروی ضد آلزایمر Lecanemab توسط شرکت ژاپنی Eisai با شراکت کمپانی آمریکایی بایوژن ساخته شده و البته رگلاتورها مجوزی برایش صادر نکردهاند.
انتشار این خبر باعث افزایش ارزش سهام شرکت بایوژن در بورس شد{لینک} اما نکته جالب اینکه این خبر یک سال پس از عرضه داروی جنجالی آدوهلم Aduhelm توسط همین دو شرکت برای مبارزه با آلزایمر منتشر میشود.
گفتنی است داروی آدوهلم به قیمت گزاف 26 هزار دلار فقط توانست ظرفیت ذهنی بیماران آلژایمری را کمتر از یک درصد بهبود بخشیده و موجب مرگ و میر و جنجال رسانهای هم شد و بسیاری علیه آن موضع گرفتند.
سازندگان دارو همچنان ادعا دارند داروی جدید Lecanemab نظریه قدیمی را ثابت میکند که از بین بردن ماده آمیلوئید میتواند با بیماری آلزایمر مبارزه کند.{داروی قبلی نیز همین بود}
داروی Lecanemab به صورت تزریقی تجویز شده و با تجمع پلاک سمی در مغز مبارزه کرده و با آلزایمر مبارزه میکند.
اما این دارو که فاز سوم آن روی 1795 داوطلب تست شده چقدر مفید بوده است؟
در این آزمایش که قبل از ارائه به رگلاتور انجام شده، به نیمی از شرکت کنندگان 10mg/kg دارو هر دو هفته یکبار داده شد. به دیگران دارونما داده شد.
محققان حافظه، قضاوت و مهارتهای حل مسئله شرکت کنندگان را قبل از شروع کارآزمایی و دوباره 18 ماه بعد اندازه گیری کردند.
نتایج نشان داد افرادی که lecanemab دریافت کردند، وضعیت روانی خود را 27 درصد کمتر از افرادی که درمان ساختگی دریافت کردند، کاهش یافتند.
اسکنها نشان داد که گروه lecanemab تجمع آهستهتری از سطوح آمیلوئید در مغز را تجربه کردند.
با این حال، عوارض جانبی قابل توجهی نیز شناسایی شد.
تورم مغز در 12.5 درصد از گروه lecanemab مشاهده شد، در حالی که در گروه دارونما 1.7 درصد بود.
دو شرکت Eisai و Biogen اصرار داشتند که در حالی که عارضه جانبی در اسکن ها ظاهر میشود، بسیاری از این موارد حاکی از بیماری نبودند.
نتایج نشان میدهد که تورم مغزی علامتدار در 2.8 درصد از افرادی که در گروه lecanemab بودند و هیچ یک از گروه دارونما مشاهده شد.
این کارآزمایی همچنین میزان ریز خونریزیهای مغزی یا خونریزیهای کوچک مغزی را ردیابی کرد.
داده ها نشان داد که این موارد در 17 درصد در گروه lecanemab و 8.7 درصد از گروه دارونما رخ داده است.
غولهای داروسازی گفتند که این ارقام در محدوده مورد انتظار قرار دارند.
Eisai به دنبال تاییدیه برای lecanemab از سازمان غذا و داروی ایالات متحده است که انتظار می رود در اوایل ژانویه تصمیم گیری شود.